Что такое каталитическое окисление окиси углерода?
Каталитическое окисление окиси углерода-это высокоэффективная технология очистки, в которой используются катализаторы для снижения энергии активации реакции, что позволяет целенаправленно превращать окись углерода и кислород в нетоксичный углекислый газ в мягких условиях. Суть этой технологии заключается в выборе подходящих катализаторов и их адаптации к конкретным условиям эксплуатации. Основные катализаторы в целом подразделяются на две группы-драгоценные металлы и недрагоценные металлы-каждая из которых подходит для различных требований различных сценариев применения. Эта технология предлагает многочисленные преимущества, включая низкие температуры зажигания, тщательную очистку, безопасность и стабильность; она широко применяется в таких областях, как очистка промышленных отработанных газов и очистка воздуха в закрытых помещениях, выступая в качестве ключевого решения для борьбы с загрязнением угарным газом.

I. Что такое каталитическое окислениеОкись углерода? (Определение и анализ)
Каталитическое окисление окиси углерода-это технология очистки газов, основанная на каталитических реакциях. Его основной принцип заключается в использовании катализатора для облегчения окислительно-восстановительной реакции между токсичным монооксидом углерода (CO) и кислородом (O₂)-без необходимости высоких температур или открытого огня-тем самым достигая целевого преобразования CO в нетоксичный и безвредный углекислый газ (CO₂). и эффективно выполняет удаление и очистку окиси углерода. По сравнению с традиционными технологиями очистки СО, такими как физическая адсорбция и высокотемпературное сжигание, эта технология предлагает значительные преимущества, включая низкое энергопотребление, высокую эффективность преобразования и отсутствие вторичного загрязнения. Следовательно, в настоящее время она является предпочтительной технологией глубокой очистки CO как в промышленном, так и в жилом секторах; она может последовательно снижать концентрацию CO на выходе до уровня ниже 5 ppm, достигая эффективности очистки в диапазоне от 95% до более 99%.
II. Основные принципы каталитического окисления окиси углерода
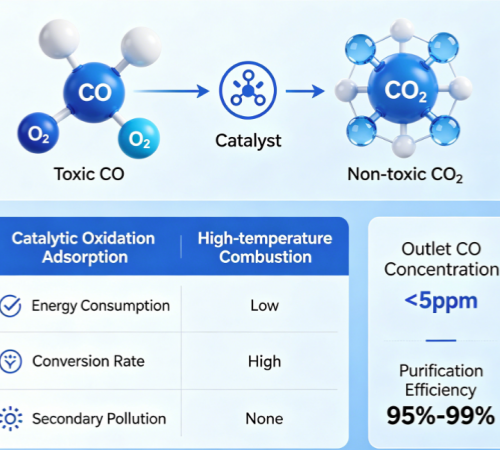
Суть каталитического окисления окиси углерода заключается в каталитическом ускорении реакции окисления СО. Его основной механизм включает катализатор, снижающий энергию активации реакции-тем самым разрушая энергетический барьер между CO и O₂-и способствуя быстрому протеканию реакции в мягких условиях. Химическое уравнение для этой реакции: 2CO + O₂ (катализатор) → 2CO ₂. Весь процесс не связан с открытым пламенем и не представляет опасности взрыва; кроме того, тепло, выделяемое в ходе реакции, может быть извлечено и утилизировано, что еще больше снижает потребление энергии. С точки зрения механизма реакции, молекулы СО сначала адсорбируются на активных центрах катализатора; после активации они реагируют с кислородными формами, адсорбированными на поверхности катализатора, с образованием CO₂. Вновь образованный CO₂ затем десорбируется с поверхности катализатора, завершая каталитический цикл. Важно отметить, что сам катализатор не расходуется во время реакции, служа исключительно для ускорения процесса.
III. Основные типы катализаторов для каталитического окисления окиси углерода

Катализаторы составляют основу технологии каталитического окисления окиси углерода; их производительность напрямую определяет эффективность реакции, рабочую температуру и применимые сценарии. В настоящее время основные катализаторы делятся на две основные категории, каждая из которых имеет различные характеристики, адаптированные к различным условиям эксплуатации. В катализаторах драгоценных металлов используются активные компоненты, такие как платина (Pt), палладий (Pd) и золото (Au), которые поддерживаются на носителях, таких как глинозем (Al2O₃) или церия (CeO₂). Эти катализаторы обладают значительными преимуществами, включая высокую активность при низких температурах, высокую устойчивость к сере и влаге и отличную стабильность. Следовательно, они хорошо подходят для сложных операционных условий, таких как условия, которые существуют в химической промышленности и на объектах по сжиганию отходов, хотя они связаныС более высокими затратами. Катализаторы недрагоценных металлов, основанные на таких материалах, как оксиды меди и марганца и оксиды кобальта, характеризуются их низкой стоимостью и обильной доступностью. Они широко подразделяются на типы температуры окружающей среды (например, катализаторы хопкалита) и типы от средней до высокой температуры. Они соответственно подходят для сред с температурой окружающей среды, таких как шахты и спасательные капсулы, и для промышленных установок со средними и высокими температурами, таких как операции по спеканию стали; однако их низкотемпературная активность и устойчивость к отравлению катализатором все еще требуют дальнейшей оптимизации.
IV. Типичные сценарии применения для каталитического окисления окиси углерода
Используя свои характеристики высокой эффективности, безопасности и энергосбережения, технология каталитического окисления окиси углерода широко применяется во многих областях для решения проблем загрязнения CO в различных условиях. В промышленном секторе он в основном используется для глубокой очистки CO, обнаруженного в дымовых газах для спекания стали, доменном газе и хвостовом газе химического процесса. Эта технология может быть интегрирована с системами десульфурации и денитрификации для достижения полного контроля нескольких загрязняющих веществ при одновременном восстановлении тепла реакции для снижения потребления энергии производства. В закрытых помещениях, таких как шахтно-спасательные капсулы, подземные гаражи и подводные лодки, это позволяет быстро удалить CO, тем самым обеспечивая безопасность персонала. В гражданском и экологическом секторах он применяется в таких областях, как очистка выхлопных газов от газовых водонагревателей, самоспасатели для пожаротушения и системы регенеративного каталитического окисления (RCO), что способствует эффективному удалению CO и обеспечивает соблюдение экологических стандартов и стандартов безопасности.
Автор: kaka
Дата: 2026.04.22





 minstrong
minstrong